導入事例 「インシリコで薬剤分子とタンパク質の相互作用を高精度に予測」 ~産学官連携で実用的なFMO創薬技術を開発 / FMO創薬コンソーシアムと「京」コンピュータの利用~
星薬科大学
福澤 薫 様
"第25回目のインタビューは、星薬科大学 薬学部 薬品物理化学教室 准教授でいらっしゃる福澤 薫先生にお話をお伺いしました。
これまでDNAやタンパク質といった生体高分子の機能を分子シミュレーションで解析するためには、主に分子力場法や分指導力学法が用いられてきました。
しかしながら分子間の相互作用は古典的力場関数では精度よく記述できない場合があり、量子力学に基づいた巨大分子計算手法が待ち望まれていました。
そこで、日本発の量子化学計算手法であるフラグメント分子軌道法(FMO法)を用いて、タンパク質と科学物質との分子間相互作用をインシリコで解析し、エネルギーを高精度で予測することで、医薬品等の効率的な分子設計を可能にすることを目的に解析手法の開発、コンソーシアムや研究会の立ち上げなど、精力的に活動されています。"
この度はよろしくお願いいたします。 実は、弊社のお客様インタビューのページは、これまで女性研究者のお話を聞けるチャンスがなかなかございませんでした。とうとう念願叶いまして初の女性研究者インタビューとなり嬉しい限りです。
まずは、 福澤先生のご研究の概要をお聞かせください。
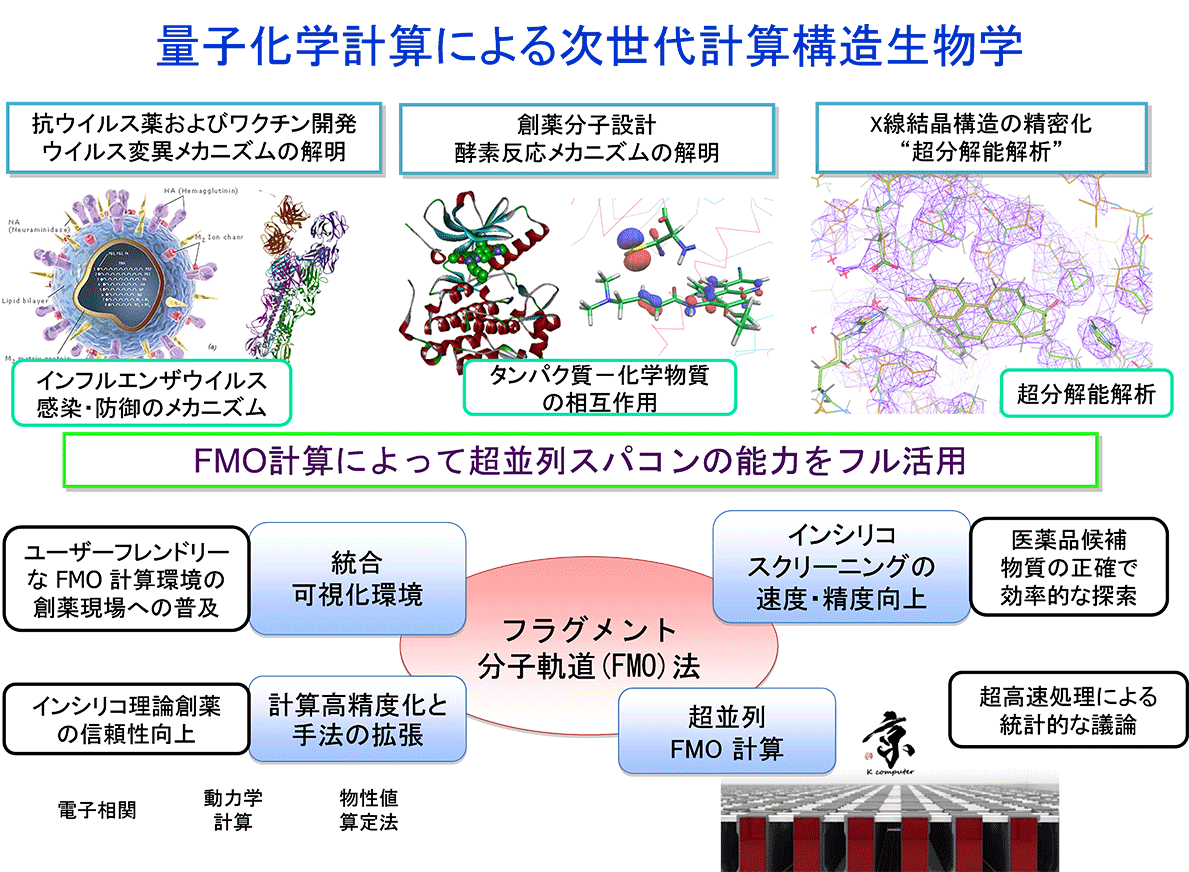
私の研究分野は、計算科学、生命科学、創薬等に関連しておりまして、主に「フラグメント分子軌道法(FMO法)」という量子化学計算手法を生命科学に応用する研究を行っています。いろいろ興味はあるのですが、最近は特に「インシリコ創薬」分野に力を入れています。タンパク質やDNAは、原子分子の世界では「巨大な分子」なのですが、FMO法では、それら巨大分子を「フラグメント」と呼ばれる小さな部分に分割して、フラグメント構造とその組み合わせの計算をすることで、分子全体の電子の状態を明らかにします。そうすることで、電子の挙動まで考慮に入れたタンパク質のシミュレーションが可能になります。
さらにFMO法の良いところは、フラグメント間の相互作用をエネルギーとして数値的に評価できることです。例えば創薬分野では、薬剤分子と創薬の標的となるタンパク質との相互作用を精密に解析することができます。タンパク質は何百ものアミノ酸から構成されているのですが、1つ1つのアミノ酸残基をフラグメントとして扱うことで、各アミノ酸と薬剤分子との「相互作用」を評価することができます。これまでに、インフルエンザウイルスや女性ホルモン(エストロゲン)の受容体、さまざまな阻害剤の標的タンパク質などに適用し、その特徴を明らかにしてきました。FMO計算から得られる情報が、高度な薬剤の分子設計に役立つことが期待されています。
広い意味での研究ターゲットは「生命科学」、手段は「計算科学」で、コンピュータをフルに使い計算量が非常に多いので、スーパーコンピュータを含めた大型計算機を使うのですが、それに伴い計算機を使いこなすためのソフトウェアの開発や、膨大な計算結果を効率よく可視化したりGUIを使って解析するための手法の開発なども行っています。 そういったものを全て駆使して計算レベルの開発や解析法などを進めつつ、応用ターゲットも研究して今に至ります。この研究に関わっている方々も大勢います。
先生はいつ頃から現在のご研究に取り組まれていらっしゃいますか?
もともと私は量子化学出身で、大学4年生で研究室に入ってからの6年間は宇宙空間の分子の計算をしていました。そこではGaussianやMolpro等のソフトウェアを使った計算が主流でした。
初めて使ったのはGaussian92で、Versionが94になった頃DFT法が入ったことでものすごく汎用性が上がりまして、研究室や分子研の計算機を使って計算するというのが爆発的に流行りました。
当時の量子化学計算といえば、数原子~十数原子程度の小さい分子化合物をターゲットにした精密計算というのが世の中のスタンダードでした。
そのような状況のなかでの私の研究テーマは、宇宙にある暗黒星雲中の星間ガスにおいて原始的な化学変化が起こっていることからそこにある「星間分子」と呼ばれる分子の計算でした。
その頃の生命科学(分子)分野は、計算は古典力場や古典分子動力学法などが主流で、アメリカを中心に古典的な手法が流行っていましたのでそれを使ってひたすら計算するという時代でした。低分子は量子力学(量子化学)、高分子は分子力学と分かれていたのですが、2000年頃からそれらが融合し始めまして、量子化学のプログラムが発展して高分子も扱えるようになりました。
1999年に現在神戸大学にいらっしゃる北浦和夫先生が日本初の理論手法であるフラグメント分子軌道法「 FMO法」を提案されました。タンパク質のように大きな分子を小さなフラグメントに分割して計算することで、計算コストを抑えながら精度よく丸ごと量子化学計算することができるという画期的な手法です。当初はGaussian94にFMO法を組み入れていたのですが、のちにGAMESSに移行して改良しながら理論開発が続いています。
一方で、国立医薬品食品衛生研究所の中野達也先生が開発されていた、ABINIT-MPという別のフリーソフトにもFMO法が組み込まれまして、国産プログラムのABINIT-MPでFMO法が使えるようになりました。私が民間企業に入社し中野先生と一緒に仕事をするようになった2000年に、ちょうど小さいタンパク質の計算ができるようになり、そこでFMO法の初めての応用計算に取り組みました。
当時はProteinDFやABINIT-MPなど、日本はタンパク質の量子計算が進んでいましたのでちょうどその時代の流れに乗って化学計算のソフトを使って最先端のことをしてきました。
もともと私は民間企業にいたこともあり、独りでコツコツと何か一つの理論を追究してきたのではなく、共同研究などを通して研究グループの中で進めていくスタイルの研究をしています。最初は2,3人での研究をしていましたが、2002年から文科省のプロジェクトである「戦略的基盤ソフトウェアの開発」が始まって以来、東京大学生産技術研究所の加藤千幸先生がセンター長を務めていらっしゃる「革新的シミュレーション研究センター」を拠点としたグループ研究を続けてきました。
それからずっとABINIT-MPと専用可視化プログラムBioStation Viewerの開発と応用のための研究プロジェクトに携わっています。これまでの一連のプロジェクトで一番大きなターゲットは「創薬」で、プロジェクトと同時平行で、製薬企業等の産業界のユーザーさんが中心になってユーザー会の運営も行ってきました。現在ではABINIT-MPの開発は立教大学の望月祐志先生を中心とするものづくり分野のプロジェクトに移行しています。
創薬と聞くと、処方箋や市場で販売されている薬をイメージしてしまうのですが、もっと基礎研究に遡ると開発のプロセスはどのような流れになるのでしょうか?
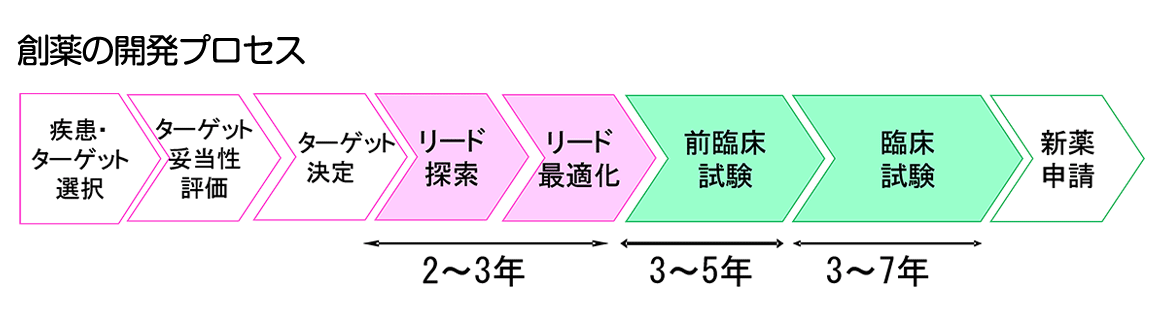
創薬の開発を最初から最後までイメージするとしたら、だいたい15年くらいの年月を経て製品化されることになります。
それまでに色々な段階があり、最終的には製品として人が使う薬となるわけですが、その手前は動物実験になりますし、その手前は、細胞実験になりますし、製品化に近くなるほど生物を扱うような実験や臨床研究になるのですが、最初の段階に遡ると、「まずどの病気(疾患)に着目するか」を決め、それが決まると、「どのタンパク質がその疾患に関わっていくのか」が特定され、「そのターゲットタンパク質に作用しそうな化合物が何か」というあたりを付ける、つまり、どのような形・性質のものがターゲットタンパク質にくっつくのか…それを探すところから始めます。
化合物を探す際には、化合物のライブラリーを用いてターゲットに結合しやすいものを探索します。あるいはデノボ(de Novo)設計でターゲットタンパク質との結合をデザインします。それが「リード探索」というフェーズになります。
これまでは実験室で「化合物」を直接扱っていた部分を、「計算機」を使って効率化しましょうというのが「インシリコ (in silico)」創薬です。データベースを使ったり、毒性の予測などに計算機を使ったりするのもインシリコですが、「インシリコ創薬」というと、だいたい「リード探索」の部分を表すことになります。 候補になりそうな化合物が見つかったらそれをより薬らしい化合物に変えていかないといけないのですが「これがくっつきそうだな」というヒット化合物が得られたときに、「もう少しここを変えたらもっとよくなるのでは?」という試行錯誤をひたすら繰り返し行います。そういうことを繰り返し、「活性」を上げていくのです。活性というのは、タンパク質のくっつきやすさを、「化合物を変形させること」で例えば1000倍にする等ですが、そこにも計算機が使われます。
学生さんがもしこの分野を研究したいと思うとしたら、きっかけとしては、「創薬への応用」というキーワードから市販の薬を想像して興味を持つものなのでしょうか?
そうですね、学生が興味を持つとしたら、計算科学的な「手法」に興味を持つ人と、「特定の疾患」に興味がある人がいると思います。
前者は「システムが好き」あるいは計算創薬の「仕組みをつくりたい」人で、後者は具体的にインフルエンザの新しい薬を開発したいというような「ターゲットに対して興味を持つ」人だと思います。インフルエンザであれば馴染み深いですし、興味を持つ人は多いです。ニュースリリースなどもしていますが、インフルエンザの話はやはり反響が大きいです。
インフルエンザのお話が出ましたので、私でもよく聞くことがあるインフルエンザの治療薬についてお聞かせいただけますか?
タミフルが一般的に認知されたのは、2009年のパンデミック(大流行)の影響がやはり大きかったと思いますし、その数年前に起きた鳥インフルエンザもそうですね。
2005年頃に、高病原性のH5N1亜型の鳥インフルエンザに人が感染した事実と、ひとたび感染すると6~7割は死に至る、という衝撃的なニュースが出てきたので、その時にタミフルの備蓄などが騒がれました。結果的に2009年にH1N1亜型という想定外の新型のインフルエンザが流行ってしまったということがありました。
あの頃からタミフルの認知度が一気に高まり流行りましたね。ただ、同時に薬剤耐性の問題も出てきて、その後はタミフル以外の治療薬も良く使われるようになりました。(現在は、リレンザに加えてイナビルも一般的な治療薬として登場)
実はタミフルよりもリレンザ(ザナミビル)の開発の方が先でした。海外で1989年に開発され、販売は1990年からしていて、日本でも2000年から販売されるようになりました。ちょうど去年の5月にリレンザ開発者のItzstein先生が日本にいらっしゃって、CBI学会のFMO研究会で一緒に講演をさせて頂きました。リレンザというのは、インシリコで論理的に作られた薬なのです。
お話を聞いていますと、先生のご研究は時代の流れに乗って着実にステップアップしているような感じですね。
そうですね(笑) 個人でやっている研究に加えて、東大生産研での一連の文部科学省のプロジェクト、JSTのCREST(5年間のプロジェクト)など、多くのプロジェクト研究に携わってきました。
会社員時代には、最先端の研究開発と同時並行で応用事例研究をして成果報告をし、GUIの開発も行ってきました。その中で多くのユーザーさんとも交流させていただき、2012年には商用化もしました。
これらの活動をする中でFMO法に関わる様々な計算手法や応用法が開発され、ユーザーが増えていき、さらに次の段階へ…ということになっていきました。大学の先生たちと一緒に研究用に開発した計算プログラムを、一般ユーザーさんがフリー版をダウンロードして使うという段階から、産学官の垣根なしに集まった皆さんで実際に計算を流し、データを解析して議論し、本当に創薬で使える手法に発展させていきましょうという段階になったということです。
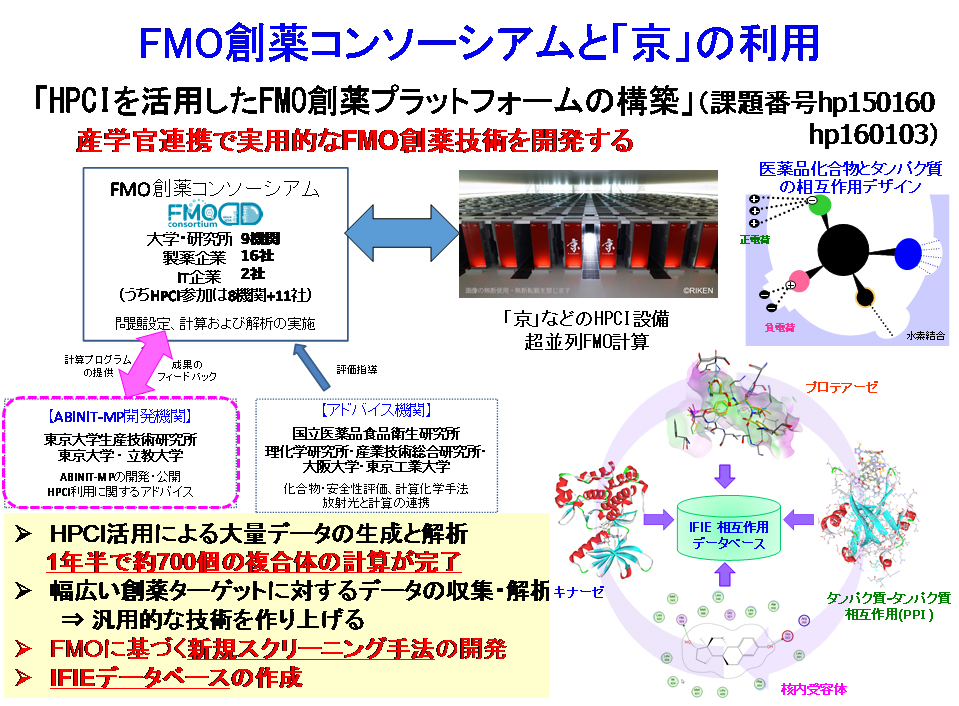
このような色々な経緯の中で、神戸大学の田中成典先生や、理化学研究所の本間光貴先生たちとFMO創薬の実現に向けた研究開発について真剣に考えるようになり、2014年の11月に私が代表者、両先生を副代表として「FMO創薬コンソーシアム」を立ち上げました。コンソーシアムの役割はプログラムの開発ではなく、ABINIT-MPあるいはFMO法を「利用して」タンパク質の計算、そして創薬に応用することです。2015年度からはスーパーコンピュータ「京」を使わせていただき、どんどん計算を流しています。
ホームページも立ち上がりここでも様々な人と関わり、仲間も増え、現在では9つの研究教育機関・18社の企業の方々と共に活動しています。
大型計算機センターを利用するにあたり、応募者が多数など、何らかの理由でこの活動ができなくなることもあるのでしょうか?
HPCI課題の申請時に「京もしくは京以外」という風に希望を出していまして、もし京の申請が通らなかった時は、九州大学スパコンセンターや、東京大学や、つくばのスパコンセンター等、他のHPCI拠点を利用させて貰うこともできるしくみになっています。
皆で集まるので大型計算機を利用しているのですが、手元で色々計算するには、居室やサーバールームなどに置いて使えるようなPCクラスターの方が使い勝手が良いと思っています。スーパーコンピュータの場合には24時間などの時間制限があり、特別なチューニングも必要ですし、パフォーマンスを出すのが難しかったりすることもある中で、時間の制限がない手元のコンピュータならもっとできるのになぁという気持ちになることもありますね。
大型計算機センターの利用は、待ち時間などはどれ位あるのですか?
ジョブキューイングシステムで順番待ちをする仕組みです。
そうなると、手元の計算機の方が順番待ちをしたり、データを持って来たり、サブミットしたり、やっと流れたと思ったらジョブが落ちたり…ということがないので、試行錯誤は手元の計算機で行い、「これで大丈夫だ!」とわかってから一式、大型計算機にジョブを投入するというやり方をしています。大型計算機のみという人はなかなかいないと思いますね。
先生は手元の計算機としてはどのようなものをお使いですか?
東大の開発プロジェクトでは、Sandy Bridgeの200コア位のマシンをよく使わせて頂いています。プロジェクトのメンバーしか使わないので、待ち時間もそれほどないですし、ジョブ制限も3日間あるので比較的使い勝手が良いです。
その他のプロジェクト関係のマシンも使えますので、共同研究者が持っているPCクラスターを使うという機会が一番多いですね。自分用としては、100コア位のPCクラスターを手元に置いておければ便利ですね。
弊社のワークステーションは昨年ご購入されていますが、使い勝手はいかがでしょうか?
購入させていただいたのは8コアの小さなマシンですが、上に述べたとおり、手元で自由に使える計算機は重宝します。御社のマシンはこれまでもいろいろなプロジェクトで使わせていただきましたが非常に使い勝手もよいです。
ソフトウェア(Amber)のインストールも自分でやるのは結構大変なので、購入時にやっていただきありがたかったです。
昨年、「第8回 資生堂 女性研究者サイエンスグラント」を受賞されたと伺っております。おめでとうございます!そのお話をぜひお聞かせ頂きたいと思います。
受賞分野が「計算化学・インシリコ創薬」・受賞研究テーマが「フラグメント分子軌道法による核内受容体のサブタイプ特異的薬剤のデザイン(副作用の少ない薬剤設計を可能にするコンピュータ創薬)」だと伺っております。
ありがとうございます。これは、資生堂が女性研究者のために研究費を支援するというものです。毎年10人選抜されますが、計算化学部門は私が初めてだったようです。これまでは医学系や生命系の実験研究者が受賞されることが多かったようですね。
受賞した研究テーマは、先ほどお話しした「FMO創薬コンソーシアム」の一端をなすものです。
資生堂に支援していただいている研究の中で扱っている、女性ホルモンの受容体タンパク質であるエストロゲン受容体は、乳がんや骨粗しょう症などのターゲットなのですが、そのタンパク質にはさらにα、βといったサブタイプに分かれています。ホルモンや薬剤、健康食品などの作用とサブタイプの関連を計算でやります!というものです。それは、「インシリコ創薬」という手段で、ターゲットが「女性ホルモンの受容体」ということになります。
同じ女性ホルモン受容体について医学的に明らかにするという人はいたとしても、インシリコという計算科学、しかも量子化学計算でアプローチするというのが初めての試みだということと、同時にコンソーシアム活動もしていますということも提案しました。
研究活動の一環としてこの女性研究者サイエンスグラントに応募したので、支援金はAmber(ソフトウェア)や、コンソーシアムのホームページ開設費用、国際会議への参加活動などに使いました。研究を発展させるために自由に使って良いという支援でしたので、有効利用させていただきました。
これから伸びそうな分野ということで注目していただけたのかなと思います。
お話を伺っていますと、長年にわたり様々な活動を精力的に活動されているイメージです!お休みされることはあるのですか?
私は子供が2人いるので出産・育児で2回お休みを取っていますよ(笑)2回合わせて1年半お休みしました。
これまでの活動は、1人でやってきたわけではなくたくさん仲間がいるので、その(皆で行っている)活動をお話しするとスケールが大きくなってしまいますが、私自身はその中のメンバーの1人として続けてきた…という感じですね。
小さなお子様がいらっしゃるとやはり育児と家事と仕事の両立は大変そうですね。ご自宅でも仕事をされることはありますか?
そうですね(笑)家でも仕事はしますね。子供もいるので、自分でも試行錯誤していますが、早朝(皆が起きる前)に仕事をしたりします。これでいける!というのはまだ決まっていないのですが色々試しています。
先生がご自宅で仕事をする姿を見ることがあるとすると、お子さんから見ても「働き者」だなぁという風に感じていそうですね!
そうかもしれませんね。子供が8歳と6歳なのですが、下の子が4歳の頃に、「ママは科学者、研究のお仕事」って言っているのを聞き、仕事のことを何となくわかっているんだなぁ…と(笑)。主人が吹き込んでいるようですが。
研究職というのはちょっと特殊なスタイルかもしれませんが、子供が、「科学者って勉強、勉強、勉強ばっかり!」って言うのを聞いて、(当時)4歳の子供の目から見て、家にいる私の様子だけを見て、「勉強ばっかりしている人」って思われていることに驚きました。実際はそうでもないところもあるのですが・・・。
やはり、精力的に仕事をしながらの子育ては尊敬します。
人によっては、家事も育児も全て自分でやるという方もいますが、時間も限られていますし、私は家族(夫)やヘルパーさんに分担してもらうようにしていますね。
男性でも同じくらい育児をしようとすると同じ事が起こると思うので、女性だけが時間に制約を受けるというのもおかしいとは思いつつも、一般的にはやはり女性の方が育児の負担が大きくなるのは否めないですね。
周りの理解も必要です。うちは家事育児を夫に手伝ってもらうというレベルではなく、二人三脚でやっています。それでも自分の時間はなかなか取れないもので、研究も思うようには進まないことも多いです。やはり、時間が自由に使えて夜遅くまででもやれる人と比べたら集中できる時間は少ないのが、なかなか難しいところですね。
子供が大きくなると手が離れるかと思いきや、先輩ママから聞くと、その時々で子育てに対して違う悩みや労力がかかるという話しなので、まだまだ先は長いですね(笑)
うまく時間をやりくりしようと考えて、「この時間にこれをしてこれをして」という時間切り分けの計画をたてても、自分の思い描いていたようにスムーズにいかないのが子育てですね。私だけが大変なのではなく子供も我慢していると思いますし、協力してくれる周りの皆さんも大変だと思いますのですごく助けられているなぁといつも思っています。
ご研究のやりがいを感じる時はどんな時ですか?
そうですね、まずは好きだから続けられているのでしょうし、純粋に「知りたい」気持ちが原動力になっています。また例えば、ソフトウェアを作って新しいことができるようになるなど、一つ一つ形になっていくところにやりがいを感じますし、誰かがそれを使ってくれて役に立つということもやりがいに繋がりますし、論文などの形で区切りがついた時もやりがいを感じますね。
研究者は皆そうだと思いますが、誰かにやれと言われるのではなく自発的にやっていると思うので、自分の書いた論文や作ったしくみを使った誰かが他で発表していて、「こんな良い結果が出ました」と言われるとそれはとても嬉しいですし、やりがいを感じる時です。
実際に創薬でも製薬企業の方が、私の研究成果を見て同様の研究を始めたと言ってくれて、しかも実際にやってみたら良い結果を得られたと言われたときにはとても嬉しかったです。
常に良い状態で研究ができるかというとそうでもないので、もうダメかな…と弱気になるときもありますが、基本的には好きなことをやっているからこそ続けられているのでしょうね。
日本の研究者のうち、女性が占める割合は、緩やかな増加傾向にはあるものの、15%以下にとどまっていると伺いました。女性研究者として、苦労を感じるのはどんな時ですか?
計算科学に関しては、ここ数年で女性研究者はだいぶ増えたように思います。少ないといわれていても集団の中で女性が1人とかいうことはあまりなくなってきました。むしろ女性の方が多い時もあります。
研究の最先端の部分で男女の違いを感じることはあまりないですね。例えば女性が書いた論文だから評価されないということはなく、完全に成果が重要視される世界なのでそのあたりで不便を感じることはまずありません。ただ、とても細かい話をすると、「名前」ですね。戸籍の名前と通称名が違うと大変なことがあります。
独身時代から研究をしているので、その時に書いた論文等含め、実績を積み重ねていきたいので結婚して名前が変わっても昔のままに統一しています。通称利用も許されているのですが、色々な書類を出すときに、何倍も労力がいるのです。
例えば、書類に「福澤」と書こうとすると、まずは通称名でいいのかという問い合わせから始まり、通称名使用のために別の書類が必要になったり、それに伴って戸籍謄本を出したりしなければいけないのです。非常勤講師の登録のために戸籍謄本が必要となると役所に行って書類を書いて、何度もやりとりをして…というのがたまにではなく頻繁に起こるので、事務処理量としてはかなり膨大になりますし、毎回そのことを気にしていないといけないのが大変です。
通称名を使うことを前提にすべてのことがスムーズにいくような仕組みをつくってほしいと思います。
海外の女性研究者と比べて何か違うところ(日本ならでは)というようなことはあるのですか?
そうですね、立ち入った話になるので、海外のことまではあまり知らないのですが、以前、「外国でも共通なんだな」思ったことはありました。
私の学生時代はキャリア女性がとても少なくて、話を聞いていると親の理解が得られないとか、両親が「女の子なんだから短大に行ったほうがいい」と言われたりするような話をよく聞きました。大学院でも、「女の子が大学院に行く必要はない」と反対されたとか、そもそもそういう風に教育されているから大学院にまで行こうとは思わないとか…そういう風潮がありました。
就職する際も、「一般職」というものがあって、一般職がある就職先に就くのが普通というような時代でした。女性で大学院以上に行くというのは家族に研究者がいたりでもしない限り理解がないということが一般的だったので、私自身も祖父が教授でしたし、「自分と同じような道に進む周りの女性は家族に研究者がいる人なのかな?」と漠然と思っていたのですが、アメリカに行ったときにルームシェアした女性研究者と話した時も、「父が教授で…」という話を聞き、やはり女性研究者というのは海外でも家族に研究者がいるという人が多いのかなと思いましたね。
現在のご研究が将来どういった形になることが理想ですか?
やっとこれまでの蓄積を新しい形で発展させようと思ってコンソーシアムを立ち上げたのでまさにこれからだと思っています。
アカデミックの中で素晴らしい研究をする人もたくさんいますが、私たちはどちらかというと「産業界における実用化」を目指しています。アカデミア創薬はもちろん、実際に製薬企業さんに活用してもらって新しい薬ができるとか、創薬のプロセスが短縮化・効率化されるとか、そのようなところに役立っていってほしいし、そのための開発でありそのための研究だと思っているので、夢としては、「実際の創薬に使えるような技術になってほしい」という思いがあります。
また、私たちの武器である量子化学は、従来の計算手法と比べて結果の情報量がとても多いため、その量子化学を使って創薬に役立ちたいと思っています。量子化学に基づいた計算創薬というのを実用化できたらいいなという思いがありまして、実際それは可能だと思いますし、力学モデルではなく電子の動きを交えた方が現実に近いので、きちんとそれを踏まえた化合物の設計や創薬に役立てたいと思っています。
それが有効だという志のもとに皆さんもコンソーシアムに参加してくれていると思うので、「何かに役立ちそう」という期待を現実に変えたいですね。
新たにやってみたいことはありますか??
インシリコ創薬のほとんどの部分は、ドッキングでタンパクにくっつくのかどうかというもの(カギと鍵穴の関係とよくいいます)で、これまでお話したFMO創薬も現状ではそのようなアプローチに倣っています。しかし例えば実際の酵素反応では、化合物がタンパク質と結合した後に「化学反応」が起こります。計算生命科学(化学)というからにはぜひドッキングだけではなく化学反応まで考慮に入れたようなことをやっていきたいと思っています。
創薬との関連で言うと、ドッキングではなく代謝とか毒性予測などに関わる化学反応に基づくテーマをやってみたいですね。化学反応、酵素反応、触媒反応など、化合物が化学反応を経て変化していくというメカニズムを明らかにして、それについて色々なことを考えるというのが量子化学の醍醐味なので。
あとは「FMO超分解能解析」というテーマがあります。計算構造生物学では、構造があって初めて計算ができます。実際の計算では、タンパク質の立体構造を表す原子座標を入力するのですが、その構造は通常、X線結晶構造解析で解いています。
先ほどお話に出たProtein Data Bank (PDB)は、タンパク質の立体構造を登録して誰でもダウンロードして使える世界的なデータベースなのですが、私たちのような分子計算は、そのPDBに登録されている構造をダウンロードして加工し、計算しています。
ただこれに問題があって、精度がそれほど高くないのです。タンパク質の方は良いのですが、化合物の周辺は特によくわからないという問題があり、そういうところを高精度化したいという狙いがあります。そのために最近やっている「超分解能解析」というのは、「X線の分解能を超える解析」という意味で、実験で見えにくい箇所をFMOや量子化学計算で補い、高精度化し、使い勝手をより良くしようという取り組みです。
この研究は実験というのはどの部分で関わってくるのでしょうか??
構造生物学というと実験室で結晶を作ってX線にあてて構造解析して明らかにするというやり方が主流なのですが、そこへのコミット(計算構造生物学)という感じになりますね。計算と実験とを融合させていくということです。
これからはビッグデータの時代ですので、このような実験の大型設備と計算の大型設備を組み合わせてやっていきましょう!という意気込みでやっています。
今後の課題はございますか?
FMO計算はとにかく情報量が膨大なので、大量のデータを整備するために「IFIEデータベースを構築する」という課題があります。ただたくさん計算したという事実だけではなく、それをデータベースにしておけば、ほかの人が同じ計算をしなくても、あるタンパク質をやりたい人が検索すれば相互作用を簡単に調べられるようになります。
公共への還元ということを考えていかないといけないですし、実際にあれば便利なので、なるべく皆が良い形で結果を残せるようにデータベースの公開の準備も着実に進めています。構造生物学の研究に必要不可欠なPDBデータベースも、今では全世界のスタンダードになっていますが、もともとは「こんなのがあったら便利だよね」という考えのもとに有志が集まってコンソーシアムのように始まったものだそうです。なので、いつかIFIEデータベースもそのようになればいいなと思っています。
ありがとうございました。弊社としましても今後も引き続き快適な計算環境をご提供できるようフォローさせていただきたいと思います。
福澤 薫 先生のプロフィール

- 研究者紹介:
星薬科大学
薬学部 薬品物理化学教室 准教授
神戸大学 客員准教授
- 主な研究テーマ:
1. 量子化学計算に基づく生体高分子の超分解能構造解析技術の開発と創薬への応用
2. HPCIを活用したFMO創薬プラットフォームの構築
3. フラグメント分子軌道法によるサブタイプ特異的薬剤のデザイン
お問い合わせ
平日9:30~17:30 (土曜日、日曜日、祝祭日、年末年始、夏期休暇は、休日とさせていただきます。)